2024年11月22日,由美国约翰霍普金斯大学、中国台湾地区国家卫生研究院、日本国立癌症研究中心、复旦大学生命科学学院等多家机构组成的国际研究团队在胸部肿瘤学领域权威期刊《Journal of Thoracic Oncology》发表题为Polygenic Risk Score and Lung Adenocarcinoma Risk Among Never-Smokers by EGFR Mutation Status: A Brief Report(多基因风险评分与EGFR突变状态对从不吸烟者肺腺癌风险的影响)的研究论文。该研究通过分析东亚地区从不吸烟女性的基因组数据,首次揭示了多基因风险评分(PRS)与EGFR突变阳性肺腺癌之间的显著关联,为非吸烟人群肺癌的预防和早期筛查提供了重要科学依据。

肺癌是全球范围内癌症死亡的主要原因,2020年约占所有癌症死亡的20%。虽然吸烟是肺癌最常见的致病因素,但全球约25%的肺癌患者从未吸烟,这一比例在东亚女性中尤为突出。在这些非吸烟人群中,肺腺癌是最常见的组织学亚型,而EGFR基因突变则是其重要的分子特征。了解非吸烟人群肺腺癌的遗传易感性及其与EGFR突变状态的关系,对于制定针对性的预防和早期筛查策略具有重要意义。
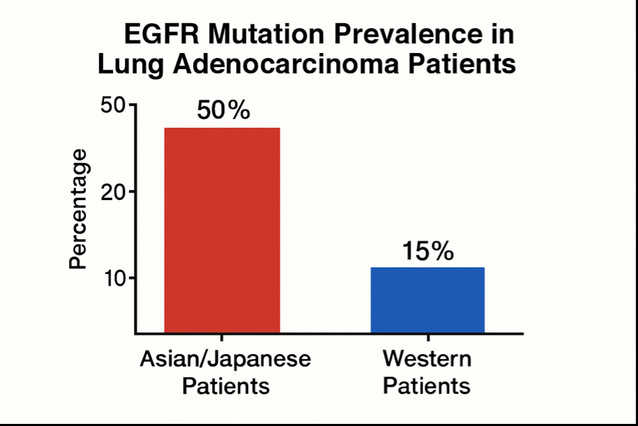
EGFR(表皮生长因子受体)是一种跨膜蛋白,负责调控细胞增殖和凋亡。EGFR基因突变是肺腺癌的重要分子特征,尤其在非吸烟者、肺腺癌患者、东亚人群以及女性中更为常见。在日本等亚洲国家,EGFR基因突变在肺腺癌患者中的检出率约为50%,远高于西方国家人群。研究团队此前已发现,在针对东亚非吸烟女性的全基因组关联研究(GWAS)中,两个易感位点rs9387478(ROS1, DCBLD1)和rs2179920(HLA-DPB1)与EGFR阳性肺腺癌的关联强于EGFR阴性肺腺癌。随着研究的深入,团队在东亚人群中共鉴定出28个独立的易感位点。本研究旨在探究基于全基因组贝叶斯方法(LDpred2)构建的多基因风险评分(PRS)是否与EGFR突变状态相关的肺腺癌风险存在差异性关联。
研究团队对来自日本、台湾、中国、香港、新加坡和韩国的998例东亚非吸烟女性肺腺癌患者(其中518例EGFR突变阳性,480例EGFR突变阴性)和4,544例非吸烟对照进行了病例-对照和多项回归分析。
研究采用了以下关键步骤:
1.基于全基因组测序数据,使用贝叶斯方法(LDpred2)构建针对肺腺癌风险的多基因风险评分(PRS)
2.根据PRS得分将研究对象分为四个等分组(Q1-Q4),以最低风险组(Q1)为参照
3.分别计算EGFR突变阳性和EGFR突变阴性肺腺癌在各PRS分组中的风险比值比(OR)
4.通过异质性检验(heterogeneity test)评估PRS对不同EGFR突变状态肺腺癌的影响差异
研究团队特别关注了PRS最高四分位组(Q4)与最低四分位组(Q1)之间的风险差异,并计算了95%置信区间和统计显著性。
研究结果显示,多基因风险评分(PRS)与EGFR突变阳性肺腺癌的关联强度显著高于与EGFR突变阴性肺腺癌的关联。具体发现包括:
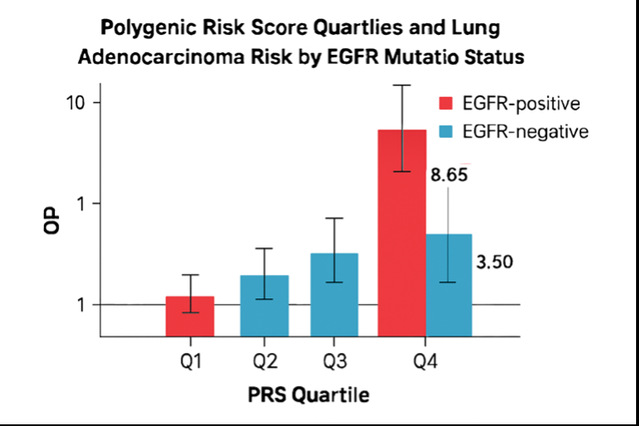
1.PRS最高四分位组(Q4)与EGFR突变阳性肺腺癌的风险比值比为8.63(95%置信区间:5.67-13.14),表明这一人群的肺腺癌风险是PRS最低组的8.63倍。
2.相比之下,PRS最高四分位组与EGFR突变阴性肺腺癌的风险比值比为3.50(95%置信区间:2.44-5.00),风险增加幅度明显低于EGFR突变阳性组。
3.两组之间的异质性检验结果显著(p-heterogeneity = 3.66 × 10^-3),证实PRS对不同EGFR突变状态肺腺癌的影响存在统计学差异。
这一发现表明,遗传易感性对EGFR突变阳性肺腺癌的影响更为显著,提示基因组背景可能通过特定的分子机制促进EGFR突变的发生或增强其致癌效应。
本研究首次证实生殖系遗传易感性可能对东亚非吸烟女性患者的肺腺癌风险产生差异性影响,这种影响取决于癌症的突变状态;多基因风险评分可能成为识别EGFR突变阳性肺腺癌高风险人群的有效工具,研究为非吸烟人群的肺癌筛查提供新的风险分层方法;此外,研究结果对东亚地区非吸烟人群肺癌的预防和早期发现具有重要意义,可能改变现有的肺癌筛查策略,进一步提高肺癌风险预测的准确性,为高风险人群提供更有针对性的预防和筛查建议。
本研究由美国约翰霍普金斯大学Batel Blechter博士、中国台湾地区国家卫生研究院Chao Agnes Hsiung教授等人共同完成,得到了日本医疗研究开发机构(AMED)革新性癌症医疗实用化研究项目、国立癌症研究中心生物银行等多项基金的支持。
论文链接:https://www.sciencedirect.com/science/article/abs/pii/S1556086424024821
